阿尔兹海默病走出“技术沉没周期”
本文系基于公开资料撰写,仅作为信息交流之用,不构成任何投资建议。
1906年,美国发明家德·福雷斯特发明了电子三极管,奠定了现代电子学的基石。然而,在人类攻破突破电子学瓶颈后,却在医药领域遇到了新的“瓶颈”。
在同年11月举行的第37届精神病学家会议上,一位名叫阿洛伊斯·阿尔茨海默的医生,向世界报告了一种全新的精神疾病。在对一例具有进行性痴呆表现的51岁女性遗体进行解剖后,他惊人的发现患者脑内遍布着大量深色淀粉样斑块。四年后,这种疾病被命名为阿尔茨海默病(简称AD)。
此后100多年的时间中,无数学者、药企在阿尔茨海默病药物研发中投入大量的时间与金钱,然而换来的却只有一个又一个的失败案例。
根据美国药物生产与研发协会发布的研究报告,仅2000-2017年间,全球累计在阿尔茨海默病药物上的研发投入就超过6000亿美元,失败的临床药物超过300种,失败率高达99.6%,占所有药物研发失败率首位。
攻克阿尔茨海默病,不仅拥有极大的财富价值,甚至已经成为当今世界医药人迫切想要实现的梦想之一。
01
AD陷入“技术沉没周期”
人们对于AD的探索,犹如盲人摸象,一直没有找到准确的方向。
认知下降,是AD的典型特征,但它同时也是自然衰老的特征之一,两者之间的最大区别在于AD会加速认知下降的速度。即使如此,但这种认知下降也是一种极为漫长的过程,很可能长达二十年时间,如此长的时间跨度造成了人类攻克AD的道路举步维艰。

图:衰老与阿尔兹海默病,来源:西部证券
尽管人类已经与AD奋战百年,但却始终没有准确找到它的发病机制,一切仍旧是个谜团。为了接近真相,科学家提出了多种假说来进行验证,如Aβ级联假说、Tau蛋白异常磷酸化假说、胆碱能假说。
但可惜的是,至今为止并没有哪一种假说得到了业界的公认,这才是为何人类在AD领域毫无收获的本质原因。
◆Aβ级联假说
淀粉样斑块是AD的主要病理特征之一,它是由Aβ沉积形成,自然也就被认为是人类攻破AD的突破口之一。Aβ级联假说成为目前最主流的AD药物研发路径。
这种假说认为,在正常生理条件下,Aβ的生成与清除处于一个动态平衡的过程,但在病理情况下,Aβ生成增多或者清除减少,导致平衡被打破。Aβ过度沉积在脑内从而引起了一系列的病理过程,这些病理过程反过来又使Aβ增多,形成了级联式的放大效应。

图:Aβ级联假说示意图
基于此,有科学家提出选择性结合和消除Aβ淀粉样蛋白聚集体的方式,以此来寻求扭转AD中的神经退行性过程。
◆Tau蛋白异常磷酸化假说
AD患者的病理特征并非只有淀粉样斑块,神经元纤维缠结也是主要病理特征之一,它是由神经原纤维异常聚集而形成的,其主要成分是高度磷酸化的Tau蛋白。

图:Tau蛋白过度磷酸化假说示意图,来源:中国银河证券
当Tau蛋白发生高度磷酸化时,可以从微管中解离出来,失去对微管的稳定作用,导致物质运输受损、神经纤维退化,从而引起AD症状。
◆胆碱能假说
胆碱能假说是最早的一种关于AD致病机理的学说。
乙酰胆碱与人的认知和记忆密切相关,而AD患者脑内的胆碱能神经元出现严重缺失的情况,中枢胆碱能神经递质不足,从而导致定向力障碍、记忆减退、行为和个性改变等。
目前已经上市的AD药物,大多数根据胆碱能假说研发的,但显然它们并没有完全解决人类在AD上的问题。
致病因素成谜、病程进展周期长、临床指标差异大、诊断难度大,AD新药研发陷入长时间的“技术沉没周期”。
02
药企“研发黑洞”
回溯药企AD研发历程,堪称一部人类药物研发失败史。
2012年,强生/辉瑞的单抗药物Bapineuzumab的III期临床试验失败;
2014年,罗氏宣告Gantenerumab的III期临床试验失败;
2016年,礼来宣告III期临床药物Solanezumab没有达到主要临床终点;
2017年,默沙东宣布停止开发BACE抑制剂药物Verubecestat;
2018年,强生宣布其终止了BACE抑制剂剂Atabecestat II/III期临床试验……
无数药企投入巨额资金却都折戟沉沙,不能不让人生出绝望的挫败感。
在2021年之前,FDA仅批准过6种治疗AD的药物,包括:他克林(Tacrine)、多奈哌齐(Donepezil)、卡巴拉汀(Revastigmine)、加兰他敏(Galantamine)、美金刚(Menantine)以及美金刚/多奈哌齐复方制剂。

图:获批上市的部分AD药物,来源:天风证券
其中,前四种都是基于胆碱能假说而开发的乙酰胆碱酶(AchE)抑制剂;美金刚为N-甲基-D-天冬氨酸(NMDA)受体拮抗剂,但这些药物都只能改善患者的症状,不能减轻AD的病理变化,也不能逆转或减缓疾病进程。
同时,目前已获批的AchE抑制剂都有不同程度的副作用。1993年获批的他克林,会损伤线粒体,抑制DNA合成蛋白质,诱导细胞凋亡,导致严重的不良反应,临床表现主要是肝毒性和胃肠道反应,最终无奈退市;多奈哌齐是我国使用最多的AD药物,其严重不良反应表现包括神经紊乱(如躁狂症、攻击性行为和暴力行为等)。
2019年,绿谷制药的甘露特钠胶囊在国内获批上市,用于治疗轻度至中度AD,改善患者的认知功能,是我国第一款治疗AD的原创新药。其作用机制是重塑肠道菌群,抑制肠道细菌氨基酸型神经炎症,从而抑制AD。
然而,该药自上市以来就一直争议不断,主要疑问指向其Ⅲ期临床试验周期过短、效果评估依据不充分、药物作用机理阐释不明、疗效曲线突变诡异等方面。因此,即使进入医保后价格大幅下降,销售额也远没有想象中的理想。
随着全球人口老龄化的加剧,AD患者数量持续升高,据World Alzheimer Report数据显示,2015年AD患者人数为4680万,预计2030年增长至7470万,到2050年时,这个数字将会达到1.3亿。
“无药可治”的困境让AD成为全球暗藏机遇最大的药物品类,也有望成为继心血管疾病、脑血管疾病和癌症之后,全球第四大药物市场。
03
百炼终成钢
传统疗法迟迟无法满足AD用药需求的情况下,人类终于在2021年取得了新的突破。
2021年6月,FDA批准渤健的Aduhelm上市,这是第一款基于Aβ级联假说的药物,也是第一款治疗AD本身的药物。Aduhelm选择性识别Aβ构象表位的免疫球蛋白G1(IgG1)单克隆抗体,与患者脑组织中的Aβ沉积结合,激活免疫系统,清除大脑中的沉积蛋白,从而影响AD发病进程。
基于临床数据,渤健向世人证明,Aduhelm可以显著使患者的淀粉样斑块减少,这也是它之所以能够获得FDA批准的原因。但这种淀粉斑块到底是不是阿尔兹海默症的诱发因素,依然存在争议,而Aduhelm并未向市场证明这一点,同时Aduhelm还存在明显的副作用,这也是它最终商业化失败的原因。
不过,Aduhelm的失败并没有让渤健放弃AD药物研发,基于Aduhelm的失败经验,渤健在两年之后带着另一款产品Leqembi重新回到大众视野,让人们再次看到了攻克AD的曙光。
2023年1月,FDA宣布完全批准由卫材和渤健联合开发的AD新药仑卡奈单抗(Leqembi),用于治疗早期AD患者的上市,成为全球首个能延缓AD进程的药物。2024年1月,该药在中国获批。
III期临床研究结果表明,与安慰剂相比,Leqembi治疗组患者CDR-SB(量化痴呆症状的各种严重程度)下降减少了27%。在意向治疗(ITT)人群的分析中评分差异值为-0.451(p=0.00005)。在安全性方面,Leqembi显著降低了脑肿胀的发生率,接受Leqembi治疗的患者中仅有13%出现脑肿胀。由于其良好的安全性数据,上市后未被添加“黑框警告”。

图:Leqembi达到了临床主要终点,来源:卫材公告
Leqembi的成功获批初步验证了Aβ假说的有效性,是AD领域药物开发的标志性事件,被认为是AD治疗的新开端。
在Leqembi上市的半年之后,礼来也实现了AD领域的突破,披露了AD新药Donanemab的最新完整3期临床数据。与安慰剂相比,接受Donanemab治疗的受试者进展到疾病下一阶段的风险降低了39%;52%的受试者在1年内达到了淀粉样蛋白斑块清除的要求,72% 的受试者在18个月内完成。
从临床研究数据来看,Donanemab的疗效更优于Leqembi,礼来也就此提交了上市申请。不过,这并没有帮助Donanemab顺利上市,FDA在今年3月份最终决定推迟Donanemab药物的上市批准,并将组织外部专家会议讨论该药物的安全性和有效性。
04
AD研发终现曙光
Leqembi的成功,打开了AD治疗领域新世界的大门,已然成为AD药物研发新路径。
接下来,各大药企或将沿着这一路径开始进行疗效和安全性的比拼。
除了Leqembi和Donanemab之外,在AD治疗领域,有127种潜在药物正在进行共164项临床试验。其中,处于III期临床阶段的试验共48项,涵盖32款药物;处于II期临床阶段的试验共90项,涵盖81款药物;处于I期临床阶段的试验共26项,涵盖25款药物。
基于Aβ假说的疗法是其中资金和研究投入最多的类型,进入临床开发的产品还有礼来的Remternetug、Annovis Bio的buntanetap、勃林格殷格翰的iclepertin、阿斯利康/ Cerveau Technologies等。
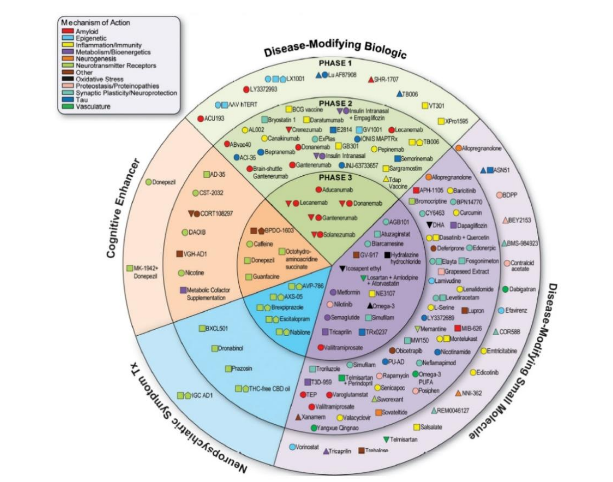
图:AD在研药物进展情况
除靶向Aβ路径外,还有其他很多研发路线也在不断取得进展,包括在糖尿病和减肥领域大放异彩的GLP-1药物司美格鲁肽,针对AD适应症的开发正处于III期临床阶段。
对于AD而言,越早发现,越早治疗,就越容易延缓病程。然而,目前尚没有针对AD的早筛产品上市。
基于这一背景,不少药企选择跳过早期诊断环节,直接研发AD疫苗,希望通过自身免疫的方式清除Aβ淀粉样蛋白或Tau 蛋白,为治疗阿尔茨海默病开辟了另一条道路。这其中,AC Immune和强生共同研发的AD的疫苗ACI-24.060于2023年6月获得FDA授予的突破性疗法资格认定,目前正在进行II期临床试验。
AD领域又燃起星星之火,有望点燃AD赛道长期被抑制的火焰,随着越来越多的资本入局,人类或将开始在AD赛道全力奔跑。
原文标题 : 阿尔兹海默病走出“技术沉没周期”

图片新闻
技术文库
最新活动更多
-
4月23日立即报名>> 【在线会议】研华嵌入式核心优势,以Edge AI驱动机器视觉升级
-
4月25日立即报名>> 【线下论坛】新唐科技2025新品发布会
-
7.30-8.1火热报名中>> 全数会2025(第六届)机器人及智能工厂展
-
7月30-31日报名参会>>> 全数会2025中国激光产业高质量发展峰会
-
精彩回顾立即查看>> OFweek 2025(第十四届)中国机器人产业大会
-
精彩回顾立即查看>> 【在线会议】从直流到高频,材料电特性参数的全面表征与测量







 分享
分享












发表评论
请输入评论内容...
请输入评论/评论长度6~500个字
暂无评论
暂无评论