进军实体瘤、缓解CRS,展望细胞免疫疗法近期新动向
当人体内大多数细胞开始不受控的分裂时,癌症就发生了。癌症这类因细胞分裂分化出现异常的疾病从古有之,而伴随着科学技术的进步,人们踏入了微观世界,开始从细胞分子角度去寻找治愈这类疾病的方法。
而目前最受青睐的技术莫过于细胞免疫疗法,人们尝试从细胞角度去消灭癌症,从赋予不同种类免疫细胞具有特异性的“火眼金睛”,来针对性的消灭某一类疾病。而CAR-T疗法是认可度最高、进展最快的细胞疗法,目前已有两款产品被批准上市(Kymriah和Yescarta)。
细胞疗法这个战队当然远远不止CAR-T这个成员,还有NK、TCR-T等细胞疗法也前景广阔。作者整理近期细胞疗法的一些新动向,共同见证细胞疗法的进步。
全球首个“CAR-T治疗艾滋病”的专利授予中国武科大两教授
11月27日,武汉科技大学生命科学与健康学院的张同存和顾潮江两位教授获得了“一种治疗HIV感染的嵌合抗原受体(Chimeric Antigen Receptor,CAR,编者注)的重组基因构建及其应用”的发明专利证书。这是全球首个应用CAR-T细胞疗法治疗艾滋病的发明应用,将为治愈艾滋病提供了新的治疗思路。

图片来源:武汉科技大学官网
张同存教授多年来一直专研在CAR-T领域,有着丰富的CAR-T临床经验,是中国CAR-T的“推广之父”,而顾潮江讲授有着对艾滋病十余年的研究经验。2015年,二人各取所长,强强联手打造“应用CAR-T技术治疗艾滋病”的新疗法。
艾滋病是一种免疫缺陷病,HIV病毒进入人体后,专门攻击人的免疫系统,免疫系统受到破坏后,人体无法抵御外界的其他病菌感染,从而患病死亡;CAR-T技术简而言之是教免疫T细胞识别特定抗原,靶向攻击病原体。
而此次研究将病毒蛋白gp120和gp41高度特异性结合的广谱中和抗体作为scFv(single-chain variable fragment,单链抗体),这种抗体能与大多数HIV病毒结合,两位教授就是用scFv的融合蛋白基因“教会”T细胞特异识别并摧毁被HIV感染的细胞,并中和血液中的HIV。
目前,通过此项技术进行的人体临床试验也效果显著,两例试验的HIV患者中,其一患者三个月体内HIV病毒大幅度降低,其二患者在治疗九个月后,体内已经完全清楚HIV病毒。此外,这项技术还能消灭处于休眠状态的被感染细胞,杜绝HIV的卷土重来。
FDA批准Fate公司NK管线IND申请
11月30日,Fate Therapeutics公司宣布FDA已经批准其在研产品FT500的IND申请,在其后的美国血液学会(ASH)上,他们公布了近期的FT500与免疫检查点PD-1药物、免疫T细胞结合使用的临床数据,数据显示99%的肿瘤都已缩小。
Fate Therapeutics是美国一家运用基本生物机制开发干细胞疗法的生物公司,成立于2007年,目前已经完成9轮融资,金额累计1.6亿美元。该公司有两大NK细胞管线,一个是从健康人外周血培养获取强杀伤力的NK细胞,另一个是从诱导多能干细胞(iPSC)分化出来具有高亲和力的NK细胞。而此次被批申请的FT500正是一种诱导多能干细胞(iPSC)的天然杀伤(NK)细胞。
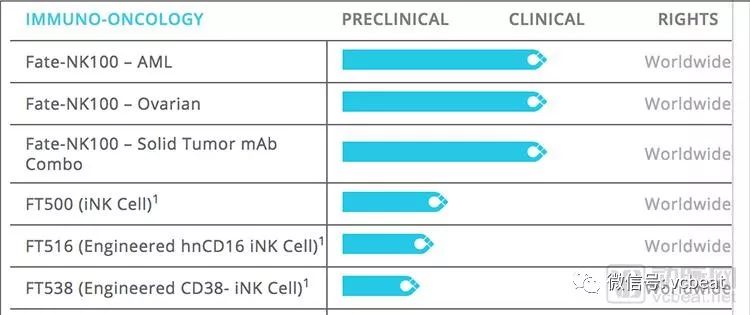
Fate Therapeutics部分研发管线
NK细胞即自然杀伤细胞(Natural Killer),是免疫系统最前线的细胞,属于先天免疫系统,具有广谱的抗肿瘤作用。FT500可以提供大量的NK细胞群,接触肿瘤上的应激配体释放出细胞毒性颗粒,使肿瘤直接裂解;同时NK细胞分泌的细胞因子可以增强T细胞活性,在T细胞协同下识别肿瘤细胞,使其消灭。此外,FT500可以进行冷冻保存,便于临床重复给药。
Fate Therapeutics首席执行官Scott Wolchko先生表示,“此次,FDA批准了FT500的IND申请,是一个重要的里程碑事件,标志着细胞产品临床开发新时代的开始。”
抑制谷氨酰胺代谢能增强CAR-T疗效
11月1日,美国范德堡(Vanderbilt)大学由Jeffrey Rathmell博士带队的生物研究小组在《Cell》杂志上发布论文,称在抑制一种名为谷氨酰胺的氨基酸代谢后,调节抗癌反应的T细胞会变得活跃,能增强细胞疗法中CAR-T的功能。

论文标题《Distinct Regulation of Th17 and Th1 Cell Differentiation by Glutaminase-Dependent Metabolism》
谷氨酰胺是人体内许多细胞维持正常功能的必要氨基酸,而异常分裂的癌细胞对谷氨酰胺的需求会更多。原实验是想通过抑制谷氨酰胺的代谢,“饿死”癌细胞。这也难免会伤及无辜,让T细胞也跟着“挨饿”——降低了活性。
然而研究结果却截然相反,在剔除小鼠的谷氨酰胺酶编码基因后,意外发现小鼠体内某些T细胞竟变得异常活跃,而这部分活跃的T细胞就是参与抗癌、抗病毒反应的T细胞。
Jeffrey Rathmell教授也对此做出了回应,简而言之就是一些T细胞需要谷氨酰胺,而另一些则不需要。需要的例如引发自身免疫的T细胞就会活性降低,而不需要的抗癌T细胞活性就会增加。在进一步进行小鼠CAR-T模型试验后,也发现在经过抑制谷氨酰胺代谢的小鼠体内,CAR-T细胞不仅体内存在时间增加,而且功能增强,不过功能增强只是短期的。
而此次实验中抑制谷氨酰胺代谢是CD-839谷氨酰胺酶抑制剂,实验小组也计划将它与免疫检查点PD-1抑制剂Opdivo联合使用,测试各种给药方案。

图片新闻
最新活动更多
-
4日10日立即报名>> OFweek 2025(第十四届)中国机器人产业大会
-
7.30-8.1火热报名中>> 全数会2025(第六届)机器人及智能工厂展
-
7月30-31日报名参会>>> 全数会2025中国激光产业高质量发展峰会
-
精彩回顾立即查看>> 【上海线下】设计,易如反掌—Creo 11发布巡展
-
精彩回顾立即查看>> 【线下论坛】华邦电子与莱迪思联合技术论坛
-
精彩回顾立即查看>> 【线下论坛】华邦电子与恩智浦联合技术论坛
-
10 DLL3领域的中国时刻







 分享
分享












发表评论
请输入评论内容...
请输入评论/评论长度6~500个字
暂无评论
暂无评论